近日,山東農業大學食品科學與工程學院江楊/李大鵬教授團隊在國際材料與界面科學領域知名期刊《ACS Applied Materials & Interfaces》在線發表題為“Hydrogel Microspheres with Gut-Adaptive Structures for Efficient Probiotic Delivery and Gut-Targeted Release”的研究性論文。
口服益生菌在調節腸道菌群、維持腸道穩態方面具有巨大潛力。然而,胃腸道的惡劣環境(如強酸、消化酶)導致益生菌存活率低,且其在復雜的腸道環境中定植率差、難以靶向作用位點,限制了其治療效果。同時,常見天然多糖水凝膠微球材料也可能存在結構強度不足、凝膠穩定性不佳等問題,導致益生菌提前釋放。
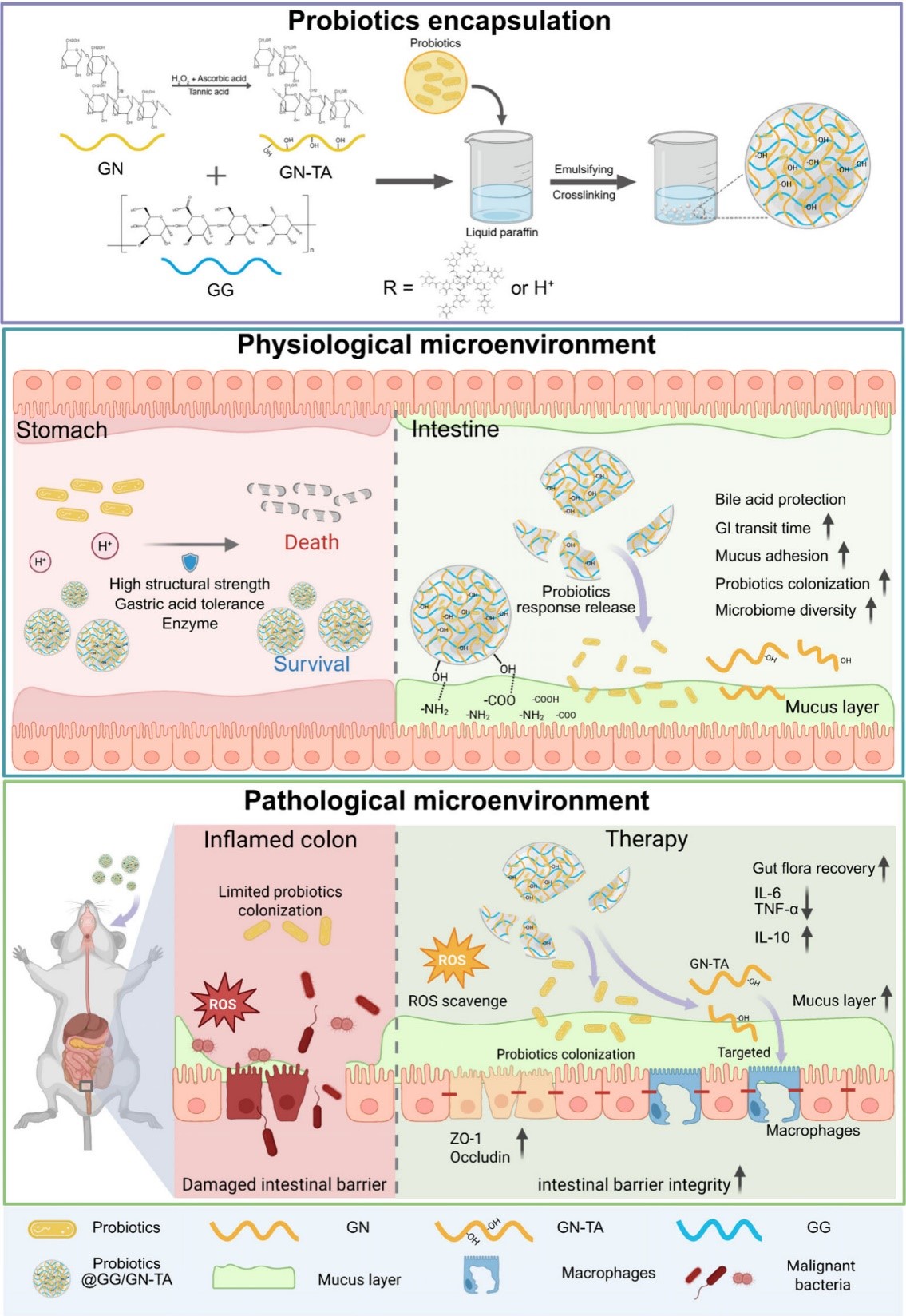
針對這一瓶頸,本研究提出了一種“結構自適應+靶向黏附”的復合策略,利用結冷膠(GG)與改性β-葡聚糖(GN-TA)構建了具有腸道適應性結構的益生菌負載水凝膠微球(GG/GN-TA HMs)。該研究利用金屬-酚類網絡(MPNs)增強了微球的結構強度,賦予其在胃酸環境下的質子化致密特性,實現了對益生菌的有效保護;同時利用β-葡聚糖(GN)的靶向性與單寧酸(TA)的黏附性,顯著提高了益生菌在腸道的滯留時間與定植效率。該成果不僅揭示了結構自適應微球對益生菌的保護機制,更為炎癥性腸病(IBD)的治療及新型口服益生菌制劑的開發提供了高效、通用的遞送平臺。
1. 腸道適應性水凝膠微球的構建與結構調控。以低酰基結冷膠(GG)為骨架,引入通過自由基接枝法制備的單寧酸接枝β-葡聚糖(GN-TA)。利用反相乳液法,結合鈣離子與TA形成的金屬-酚類網絡(MPNs),成功制備了具有雙重網絡結構的GG/GN-TA水凝膠微球。300 mM Ca2?條件下的GG/GN-TA微球在測試中表現出更強的機械強度與結構適應性,具有優異的自愈合能力與抗形變能力,有助于抵御食品加工及胃腸蠕動過程中的剪切力。
2.pH響應性結構自適應與多重保護機制。①結構自適應保護:在胃酸環境(低pH)下,微球中的羧基發生質子化,誘導網絡結構收縮致密,有效阻滯了H+的滲透,從而為益生菌提供了“盾牌”式保護。在模擬胃液消化及長期儲存條件下,負載于GG/GN-TA微球中的雙歧桿菌(Bifidobacterium animalis)與大腸桿菌Nissle 1917(EcN)存活率顯著高于游離菌及純GG微球組。②腸道靶向與黏附:當微球進入腸道(中性pH)后,羧基解離導致網絡溶脹,孔徑增大,促進益生菌釋放。同時,GN-TA組分中的單寧酸提供了豐富的鄰苯二酚基團,賦予微球優異的黏膜黏附性;而β-葡聚糖則能特異性識別巨噬細胞表面的Dectin-1受體,實現了對炎癥部位的主動靶向。
3.顯著的結腸炎治療與菌群調節效果。在DSS誘導的結腸炎小鼠模型中,負載EcN的GG/GN-TA微球(EcN@GG/GN-TA)展現出卓越的治療功效。緩解炎癥與修復屏障:EcN@GG/GN-TA顯著降低了小鼠體內促炎因子水平,抑制了氧化應激,并上調了緊密連接蛋白的表達,有效修復了受損的腸道黏膜屏障。重塑腸道菌群:16S rRNA測序結果表明,該遞送系統具有“合生元”協同效應。GN-TA作為益生元被腸道菌群利用,顯著提高了毛螺菌科等產短鏈脂肪酸(SCFAs)有益菌的豐度,恢復了腸道微生態平衡。相比于單一療法,EcN@GG/GN-TA在防止體重下降、改善疾病活動指數(DAI)及維持結腸長度方面效果最佳。
該研究創新性地將具有益生元特性與免疫調節功能的改性多糖(GN-TA)引入水凝膠體系,通過金屬-酚類網絡交聯,構建了集“物理屏障+靶向黏附+合生元協同”于一體的新型益生菌遞送系統。該體系制備方法簡單、原料均為食品級、生物相容性好,不僅適用于多種益生菌的包埋,也為開發針對潰瘍性結腸炎(UC)等腸道疾病的功能性食品與口服藥物制劑提供了具有廣闊應用潛力的新策略。
原文鏈接:https://doi.org/10.1021/acsami.5c22342.
編 輯:萬 千
審 核:賈 波









