近日,動物醫學院商營利教授課題組在《Communications Biology》上在線發表了題為“Retinol binding protein 4 restricts PCV2 replication via selective autophagy degradation of viral ORF1 protein”的研究論文。該論文揭示了宿主因子視黃醇結合蛋白RBP4通過激活選擇性自噬調控豬Ⅱ型圓環病毒(Porcine circovirus 2,PCV2)復制的新機制。
PCV2是導致豬PCV相關疾病的主要病原體,是已知感染哺乳動物的最小病毒,其單鏈環狀DNA基因組大小約為1.7 kb。PCV2主要感染宿主免疫細胞,造成免疫抑制,給全球養豬業造成了巨大經濟損失。由于其基因組小,PCV2復制嚴重依賴于免疫細胞機制,與許多宿主細胞因子相互作用。特別是PCV2可以在豬體內持續存在,并駐留在某些免疫細胞如巨噬細胞和樹突狀細胞中,進而調節其功能。但目前對于PCV2在靶細胞中維持持續低水平復制的機制尚不清楚。
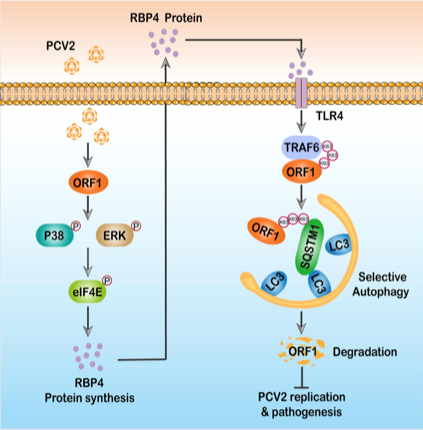
在本研究中,研究人員發現PCV2感染宿主細胞后能夠活化MAPK-eIF4E信號通路從而誘導RBP4蛋白水平顯著升高,RBP4升高后能夠顯著抑制PCV2的復制,而RBP4缺失后促進病毒復制。RBP4做為一種分泌型細胞因子,在胞內合成后能夠分泌至胞外,以反饋的方式抑制PCV2的復制。深入研究表明,RBP4通過激活自噬受體SQSTM1/p62介導的PCV2病毒蛋白ORF1的選擇性自噬降解,進而抑制PCV2的復制。進一步研究發現,RBP4通過活化TLR4信號通路活化下游的E3泛素連接酶TRAF6,從而觸發SQSTM1/p62介導的選擇性自噬,促進K63介導的病毒復制相關蛋白ORF1的泛素化降解。該研究結果證實RBP4是一個PCV2的關鍵宿主限制因子,揭示了宿主細胞防御PCV2感染的新機制。該項研究為深入理解PCV2的發病機制以及新型抗病毒藥物研發提供了重要理論依據。
商營利課題組已畢業博士生韓慶兵為論文第一作者。山東省人獸共患病重點實驗室、山東農業大學動物醫學院商營利教授為該文章通訊作者。商營利課題組博士后陳萌、博士生趙鶴嬌、碩士生薛文碩參與了該項研究。山東省農業科學院李俊研究員和中科院微生物所孫蕾研究員為該研究提供了重要幫助。該研究得到了山東省重大科技創新工程和山東農業大學高層次人才引進等經費的資助。
全文鏈接:https://www.nature.com/articles/s42003-024-07052-1
編 輯:萬 千
審 核:賈 波









